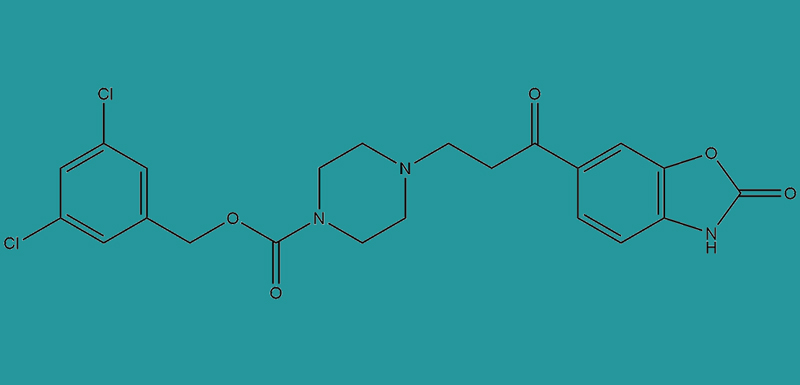
一种免疫调节抑制剂泊马度胺(Pomalidomide)
泊马度胺是沙利度胺的衍生物,具有抗血管生成作用,也可以作为免疫调节剂。泊马度胺属于一类重要的分子,是免疫调节药物(IMiD)类的第三代成员,除了其免疫调节和抗血管生成活性外,泊马度胺还具有针对骨髓瘤细胞的直接活性,影响基因表达,促进细胞凋亡和细胞周期停滞。
免疫调节药物(IMiD)作用机制主要包括调节免疫系统、抑制肿瘤细胞生长和促进肿瘤细胞凋亡。IMiD广泛应用于癌症的临床治疗,IMiD 可刺激 T 淋巴细胞增加 IL-2 分泌并减少促炎细胞因子的表达。IMiD在包括多发性骨髓瘤在内的多种癌症的治疗中发挥了关键作用。如IMiD 与 E3 连接酶 cereblon (CRBN) 结合,并将其蛋白质降解信号的能力重定向至新底物,从而去除多发性骨髓瘤相关蛋白质并提供所需的治疗效果。IMiD 是异双功能降解剂开发中用于靶向 E3 连接酶的最常用配体之一,和 E3 连接酶配体的快速合成对于新 PROTAC 的探索和优化非常重要,特别是在临床前开发阶段。
典型的 IMiDs 药物包括沙利度胺(Thalidomide)、依托利胺(Lenalidomide)和来那度胺(Pomalidomide)。这些药物在多发性骨髓瘤患者中被广泛使用,它们通过多种方式影响免疫系统的功能,以达到抗癌的效果。
Pomalidomide是美国Celgene公司生产的第三代IMiD。它是在第一代IMiD沙利度胺的基础上开发的,修改了分子结构。泊马度胺的化学名称是4-amino-2-(2,6-dioxoperidine-3-ylisoindole-1,3-diketone)。这种改进的IMiD可以增强T细胞和NK细胞介导的免疫反应,抑制单核细胞促炎细胞因子的产生,并诱导癌细胞凋亡。
泊马度胺的合成工艺改进研究
泊马度胺,CAS号为:19171-19-8,分子式为:C13H11N3O4,英文名字为4-amino-2-(2,6-dioxopiperidin-3-yl)-2,3-dihydro-1H-isoindole-1,3-dione,近年来,泊马度胺的分子结构常被用作PROTAC生产中E3连接酶的配体,在蛋白酶降解药物的开发中发挥着重要作用。筑药网可以为医药研发科研机构提供高质量的医药中间体产品、PROTAC linkers、E3连接酶配体产品、小核酸药物和ADC药物研发所需的分子砌块产品现货及产品定制服务。
有研究者为了解决制备异双功能泊马度胺缀合物的方法依赖于通常产率低且产生难以处理的副产物的问题,探索了可靠且简洁地制备泊马度胺连接子的策略,这对于这些偶联物的形成至关重要。与现有文献方法相比,研究者以高产率制备了 18 种泊马度胺连接子,提供了一种适合快速制备缀合物库的方法,而这正是开发新的蛋白质降解剂经常需要的[1]。
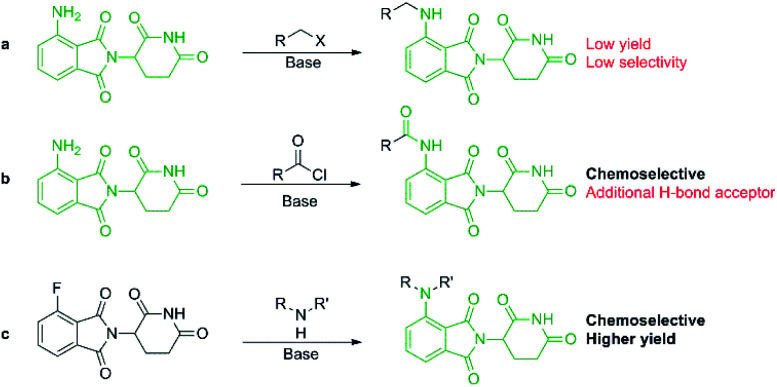
可用于制备泊马度胺衍生物的合成路线:(a)用烷基卤化物将泊马度胺烷基化,(b)泊马度胺酰化,和(c)4-氟沙利度胺的亲核芳族取代以形成泊马度胺衍生物[1]。
也有研究者对现有泊马度胺合成工艺进行分析改进,采用以3-硝基邻苯二甲酸酐为原料,经五步反应合成泊马度胺的方法。结果总产率为58.7%,泊马度胺结构由IR,1H-NMR与MS确证。结论本文涉及改进的合成工艺中,反应原料价廉易得;产率较高;反应条件温和;后处理简单;无特殊设备要求[2]。
为了改进抗肿瘤药泊马度胺的合成工艺,有研究者以N,N'-羰基二咪唑(CDI)为缩合剂环合,再用溴化氢醋酸溶液脱去苄氧羰基(CBZ)并成盐制备得到3-氨基哌啶-2,6-二酮氢溴酸盐,3-氨基哌啶-2,6-二酮氢溴酸盐再与3-硝基邻苯二甲酸酐缩合,钯碳还原硝基制得泊马度胺.该工艺具有制备简便,生产周期短,无需高压加氢反应,产品纯度高等优点,解决了泊马度胺规模化生产中存在的问题[3]。
目前针对泊马度胺合成工艺改进的研究有很多,通过泊马度胺的生产工艺优化和质量控制,不仅有助于提高泊马度胺的产率,还可以确保泊马度胺中的杂质和副产物得到有效控制,从而提高药物的安全性和有效性。
泊马度胺在多发性骨髓瘤、神经系统疾病和心脑血管疾病上的临床前研究
有研究者探讨了不同浓度的泊马度胺对人多发性骨髓瘤细胞株MM1.S的作用及对CRBN表达的影响。应用CCK-8法检测泊马度胺对MM1.S细胞增殖抑制作用;Annexin V-FITC/PI双染流式细胞术检测MM1.S细胞凋亡率;实时定量PCR检测CRBN基因表达水平;Western blot法检测泊马度胺对MM1.S细胞CRBN蛋白表达的影响。研究结果发现泊马度胺对MM1.S细胞具有抑制作用,其增殖抑制作用呈时间和剂量依赖性(r=0.981,r=0.990)......泊马度胺能够抑制MM1.S细胞增殖并促进其凋亡,一定浓度泊马度胺可降低MM1.S细胞CRBN基因表达并下调其蛋白表达水平[4]。
有研究者探讨了泊马度胺(Pom)通过TLR4/NF-κB通路对帕金森病(PD)小鼠模型的作用机制。研究者将雄性C57BL6小鼠随机分为正常对照组(Control组)、MPTP组、泊马度胺组(Pom组).MPTP组、泊马度胺组模型均腹腔注射1-甲基-4-苯基-1,2,3,6-四氢吡啶(MPTP)构建模型,对各组模型小鼠进行行为学评价.免疫荧光染色测定脑内活化的小胶质细胞,Western blotting检测炎症因子、TLR4/NF-κB通路蛋白等的表达.研究结果发现与MPTP组小鼠相对比,Pom组小鼠神经功能明显改善,小胶质细胞活化的数量明显减少,且炎症因子的表达显著降低,差异有统计学的意义(P<0.05).该研究发现泊马度胺可以通过TLR4/NF-κB通路抑制帕金森病小鼠小胶质细胞的增生,减少炎症因子的表达,有效改善帕金森病小鼠的神经功能[5]。
也有研究者探讨泊马度胺对大脑中动脉闭塞模型(middle cerebral artery occlusion,MCAO)小鼠的神经保护作用及相关机制。将雄性C57/BL6小鼠采用线栓法制成MCAO模型,成功模型随机分为假手术组(Sham组)、MCAO组、溶剂组(Vehicle组)和泊马度胺组(Pom组)。采用改良的神经功能缺损评分(mNSS)评估小鼠神经功能缺损程度,免疫荧光染色测定脑梗死灶周围增生的小胶质细胞,Western blotting检测炎症因子、神经营养因子的表达。研究结果发现同Vehicle组小鼠相对比,Pom组小鼠神经功能明显改善,小胶质细胞活化的数量明显减少,且炎症因子的表达显著降低,而神经营养因子表达增高,差异具有统计学的意义(P<0.05)。因此 泊马度胺可通过抑制脑梗死后小鼠的小胶质细胞的增生,减少炎症因子的表达,还可以产生神经营养作用,有效改善脑缺血小鼠的神经功能从而产生神经保护作用[6]。
目前无论是针对泊马度胺的合成工艺,还是杂质研究以及药理药效研究、毒副作用上的研究都有很多,展望未来,我们期待科学家们能够利用泊马度胺的基本机构研发出更安全和更有效的化合物,以广泛地应用于疾病的治疗,造福人类。
参考文献:
[1]Brownsey DK, Rowley BC, Gorobets E, Gelfand BS, Derksen DJ. Rapid synthesis of pomalidomide-conjugates for the development of protein degrader libraries. Chem Sci. 2021 Feb 3;12(12):4519-4525. doi: 10.1039/d0sc05442a. PMID: 34163717; PMCID: PMC8179520.
[2]陈仕魁. 泊马度胺的合成工艺改进[J]. 海峡药学,2015(5):261-262.
[3]朱小锋,王信见,李靖,等. 泊马度胺的工艺改进[J]. 大陆桥视野,2017(4):56-57. DOI:10.3969/j.issn.1671-9670.2017.04.046.
[4]樊文静,范枝俏,潘耀柱,等. 泊马度胺的抗骨髓瘤细胞株MM1.S活性及对CRBN表达的影响[J].中国实验血液学杂志,2019,27(6):1907-1911. DOI:10.19746/j.cnki.issn1009-2137.2019.06.032.
[5]王梦涵,卢宏. 基于TLR4/NF-κB通路探讨泊马度胺对帕金森病小鼠的作用机制[J]. 中国实用神经疾病杂志,2023,26(5):529-533. DOI:10.12083/SYSJ.230557.
[6]王梦涵,张丽敏,杨贺城,等. 泊马度胺改善脑缺血小鼠神经功能的机制研究[J]. 中国实用神经疾病杂志,2022,25(2):133-138. DOI:10.12083/SYSJ.220444.


.jpg)