2型糖尿病(T2DM)是一种进行性疾病,随时间推移,β细胞功能进行性减退,且产生胰岛素抵抗,导致常规药物治疗难以长期良好控制血糖。为了更好地控制血糖,各种降糖药物一直不断研发中。降糖策略也从以“控制血糖”为中心转向以“改善心血管功能”为中心的兼顾控制血糖模式。胰高血糖素样肽-1(GLP-1)受体(GLP-1R)激动剂兼具降糖、降血压、减轻体重及血管保护等多重生理作用,因此靶向GLP-1R开发降糖药的热潮不断,是近年来糖尿病药物研发领域的热点。
美迪西在GLP-1药物的一站式研发服务方案制定中与客户深入交流,将每一个案例的特点与多年实战经验和技术积累相结合,谨慎地将优质实验方案与结果交到客户手上。美迪西可以为客户提供GLP-1药物发现、GLP-1药学研究(原料药工艺开发+制剂)、GLP-1药效学研究、GLP-1药代动力学评价和GLP-1安全性评价等服务。截至2023年6月底,美迪西已成功助力8个GLP-1药物获批临床,其中3个GLP-1药物NMPA/FDA同时获批,1个GLP-1药物获得美国FDA、中国NMPA、澳洲TGA三国批准,另外有多个GLP-1项目在研。
GLP-1是1983 年发现的第二种肠促胰岛素,由胰高血糖素原基因编码合成, 主要由肠道 L 细胞产生。GLP-1在人体内以GLP-1(7-36)和GLP-1(7-37)两种活性形式存在, 人体内主要以含30个氨基酸的GLP-1(7-36)为主,其次为GLP-1(7-37)。
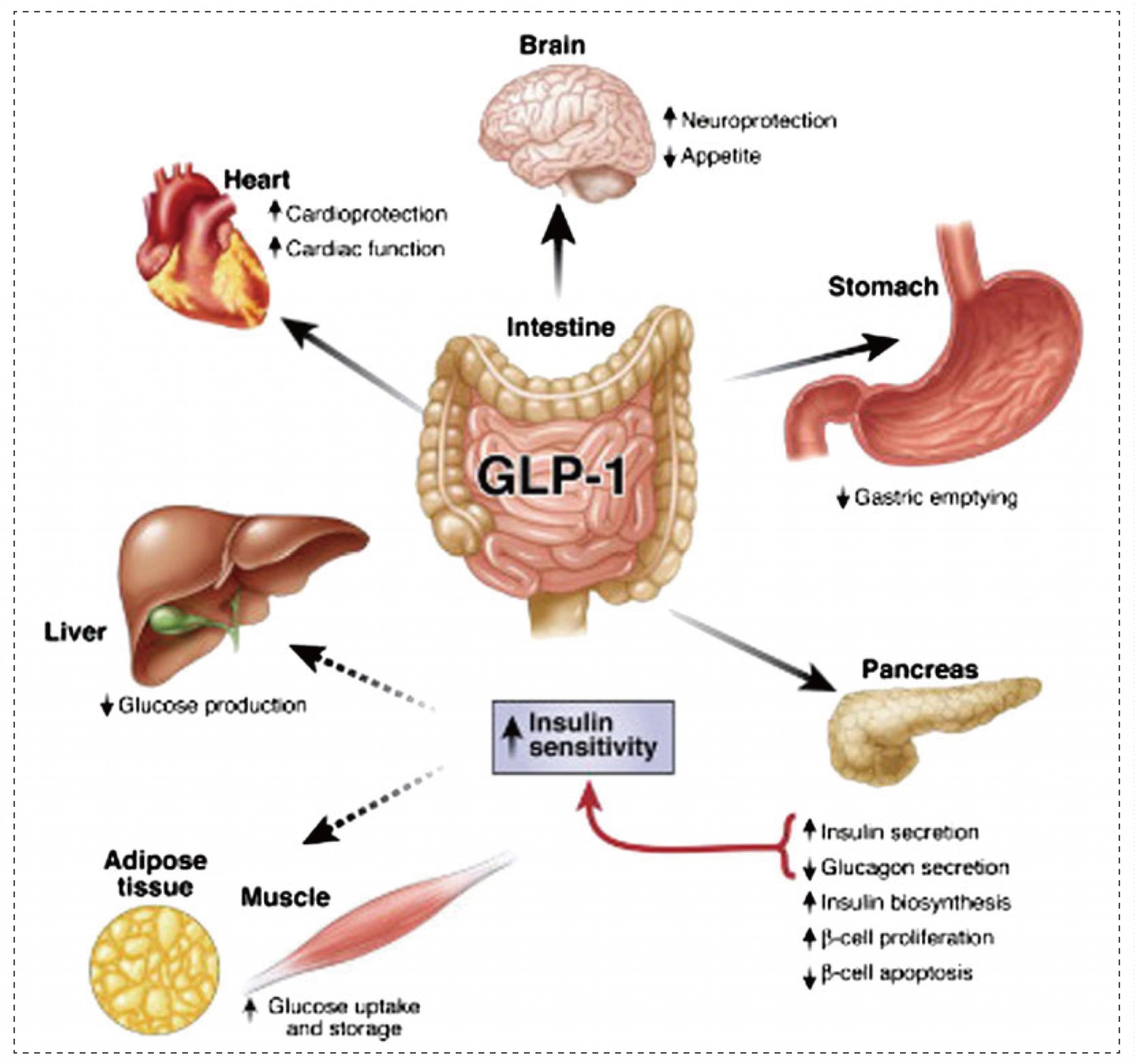
GLP-1通过与GLP-1R特异性结合,靶向胰岛细胞,刺激胰岛素分泌,且抑制胰高血糖素分泌,从而促进葡萄糖的新陈代谢。同时GLP-1还能够能延缓胃排空和抑制食欲。GLP-1在不同组织中表现出多种作用,具有广泛的治疗潜力。因此,GLP-1在糖尿病的治疗和发病机制研究中起着非常积极的作用。
GLP-1的多重生理功能[1]
目前基于GLP-1的糖尿病药物主要集中在二肽基肽酶4(dipeptidyl dipeptidase-4,DPP-4)抑制剂、GLP-1R激动剂、GLP-1类似物三个方面。DPP-4使 GLP-1 失活。口服有效的DPP-4抑制剂,有西格列汀、维格列汀、沙格列汀、利格列汀、阿格列汀等,这类药物也称为格列汀类药物,可与二甲双胍、辛伐他汀相结合联合使用。根据作用时间长短,GLP-1类药物分为长效制剂(每周注射一次:如缓释艾塞那肽、阿必鲁肽、度拉鲁肽、他司鲁肽)和短效制剂(每天注射一次或两次:如艾塞那肽、利拉鲁肽、利西拉肽)。
GLP-1R激动剂和DPP-4抑制剂有多种区别:
❖给药方式:前者皮下注射、后者口服摄入
❖疗效:GLP-1激动剂效果更好
❖对体重的影响:GLP-1R激动剂降低体重、DPP-4抑制剂对体重基本无影响
❖耐受性:使用GLP-1R激动剂会出现恶心和食欲下降、DPP-4抑制剂基本无影响
❖……
GLP-1R激动剂和DPP-4抑制剂对心血管系统都具有保护作用。在二甲双胍单药治疗失败后,格列汀类药物可作为磺脲类或格列酮类药物的有潜力的替代品,而在双重口服药治疗失败后,GLP-1R激动剂可作为胰岛素的良好替代品,尤其针对肥胖患者。GLP-1静脉给药后的半衰期一般约为 1-2 分钟,随后被DPP-4迅速降解,而失去活性。
 GLP-1R激动剂和DPP-4抑制剂的区别[1]
GLP-1R激动剂和DPP-4抑制剂的区别[1]
GLP-1R是2型糖尿病的关键治疗靶点。众多靶向GLP-1R的药物已进入临床治疗阶段。GLP-1R 与其他四种胰高血糖素受体(GCGR、GLP-2R、GIPR 和 GHRHR)属于B1类GPCR(分泌素家族),其内源性配体是肽类激素。
GLP-1R是一种多效性偶联受体,主要通过与多种G蛋白(Gαs、Gαi、Gαo和Gαq/11)偶联来调控细胞通路。当与GLP-1结合后,GLP-1R在胰岛β细胞中偶联Gαs蛋白,激活腺苷环化酶 (AC),促使cAMP在细胞内含量升高,cAMP可激活蛋白激酶A(PKA)和cAMP调节的鸟嘌呤核苷酸交换因子2(Epac2),激活后的 PKA 可以关闭 ATP 依赖的 K+通道,使细胞膜去极化。激活后的PKA还可以激活电压依赖的Ca2+通道(VDCC),使 Ca2+内流并产生动作电位。而激活后的Epac2可以激活Ras蛋白1(Rap1)和磷脂酶C(PLC),从而激活IP3和二酰甘油(DAG)途径,促进细胞内Ca2+释放,这些途径最终都会刺激血糖依赖性胰岛素的分泌。
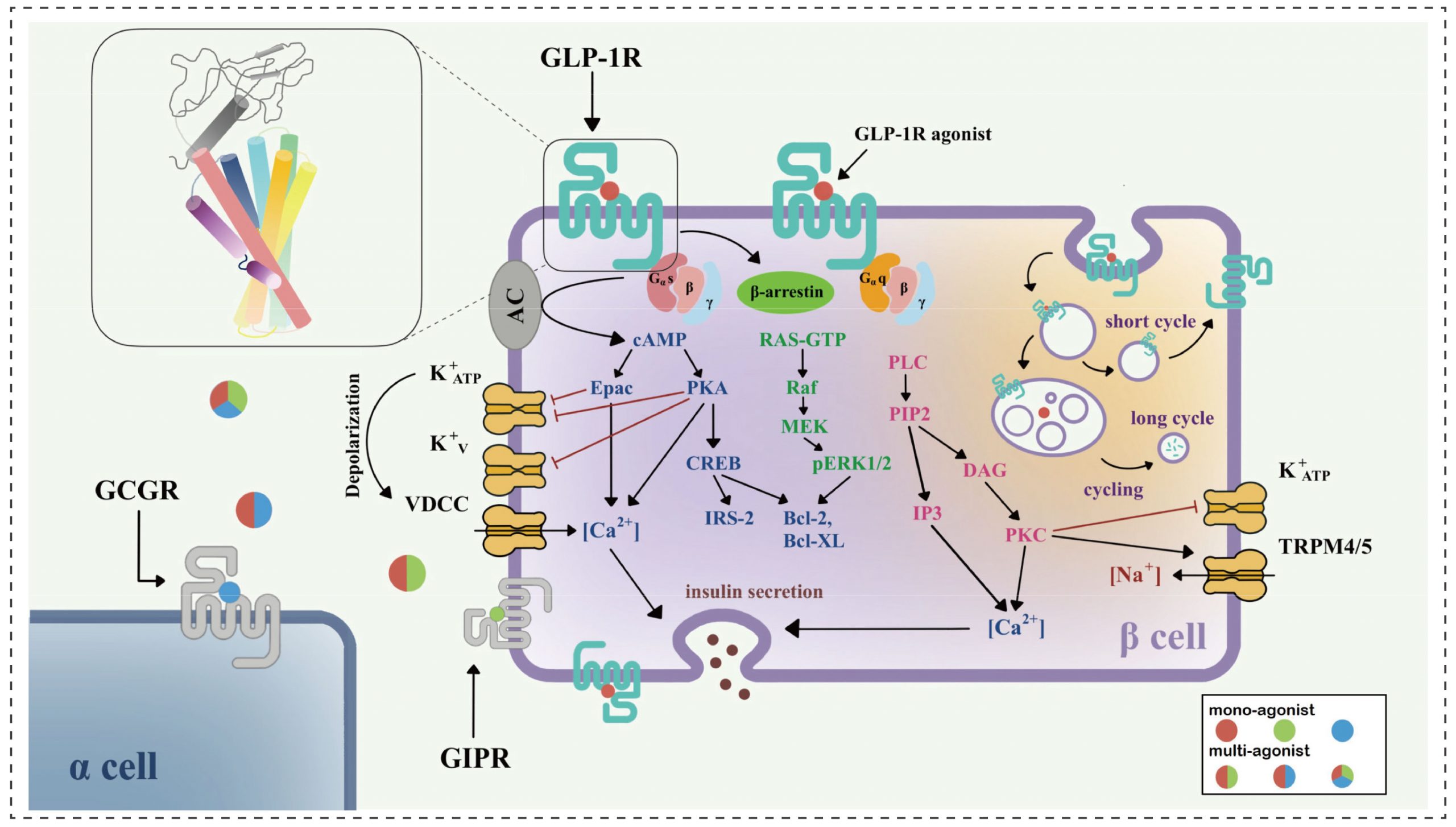 GLP-1R在胰腺β细胞中的信号通路[2]
GLP-1R在胰腺β细胞中的信号通路[2]
目前大约80%的蛋白多肽药通过注射途径给药。为改善多肽类药物稳定性,延长多肽药物的体内半衰期,使其长效化,除了对多肽进行分子结构的改造,如采用氨基酸替代或环化、PEG修饰、融合长效化片段(与Fc融合、与人血清白蛋白融合)、缀合脂肪酸链等策略。还可通过制剂学手段改善多肽类药物的吸收并使其长效化,能够有效缩短药品研发周期、降低药品研发成本,也可能为药物使用开发新的适应证。
注射型多肽药物主要制剂类型为冻干粉。近年来,随着各种递药系统的发展,研究人员开发了多肽药物多种不同的制剂类型,呈现出多种给药途径。目前多肽药物制剂有注射用微球、植入剂、缓释脂质体、微乳、纳米粒、口服长效片剂/胶囊剂 、口服微粒、 微针贴剂 、经皮微粒给药系统等。如:艾塞那肽 (Exenatide) 是由美国FDA批准的第1个GLP-1R激动剂类多肽药物,其由39个氨基酸组成。用于改善2型糖尿病患者的血糖控制,其普通剂型需每天两次进行皮下注射;随后,Amylin制药公司以聚乳酸-羟基乙酸共聚物(PLGA)为载体,成功开发了每周仅需注射1次的艾塞那肽缓释微球 (Bydureon),并于2011年和2012年先后获得欧盟和美国FDA批准。
美迪西可提供GLP-1药物的原料药工艺开发和制剂研发服务。在确保研发质量的基础上,美迪西团队通过严谨的试验方案设计(DOE)、专业化的研发技术、标准化的项目管理、规范化的试验操作、高效的多方沟通,持续助力客户的GLP-1药物研发!
美迪西多年来深耕动物领域,为药物研发提供合适的动物模型,可提供多种用于评估GLP-1药物的糖尿病模型及肥胖模型,在AAALAC认证的环境下完成模型动物的建模和饲养,并以GLP-like的高标准完成相关药效学评价试验。
这项研究是在一小部分选定的血糖正常健康受试者中进行的。本次研究由中南大学湘雅药学院、南京医科大学第一附属医院、盛世泰科生物医药技术(苏州)有限公司、北京诺和德美医药技术有限公司联合进行,其中活性GLP-1检测通过美迪西进行。实验结果表明,盛格列汀(Cetagliptin)在剂量≥50mg时每天给药一次表现出最小的积累,在24小时给药间隔内抑制血浆DPP-4活性达到80%以上,且增加活性GLP-1水平而不产生低血糖。且盛格列汀(Cetagliptin)具有良好的临床耐受性和安全性。
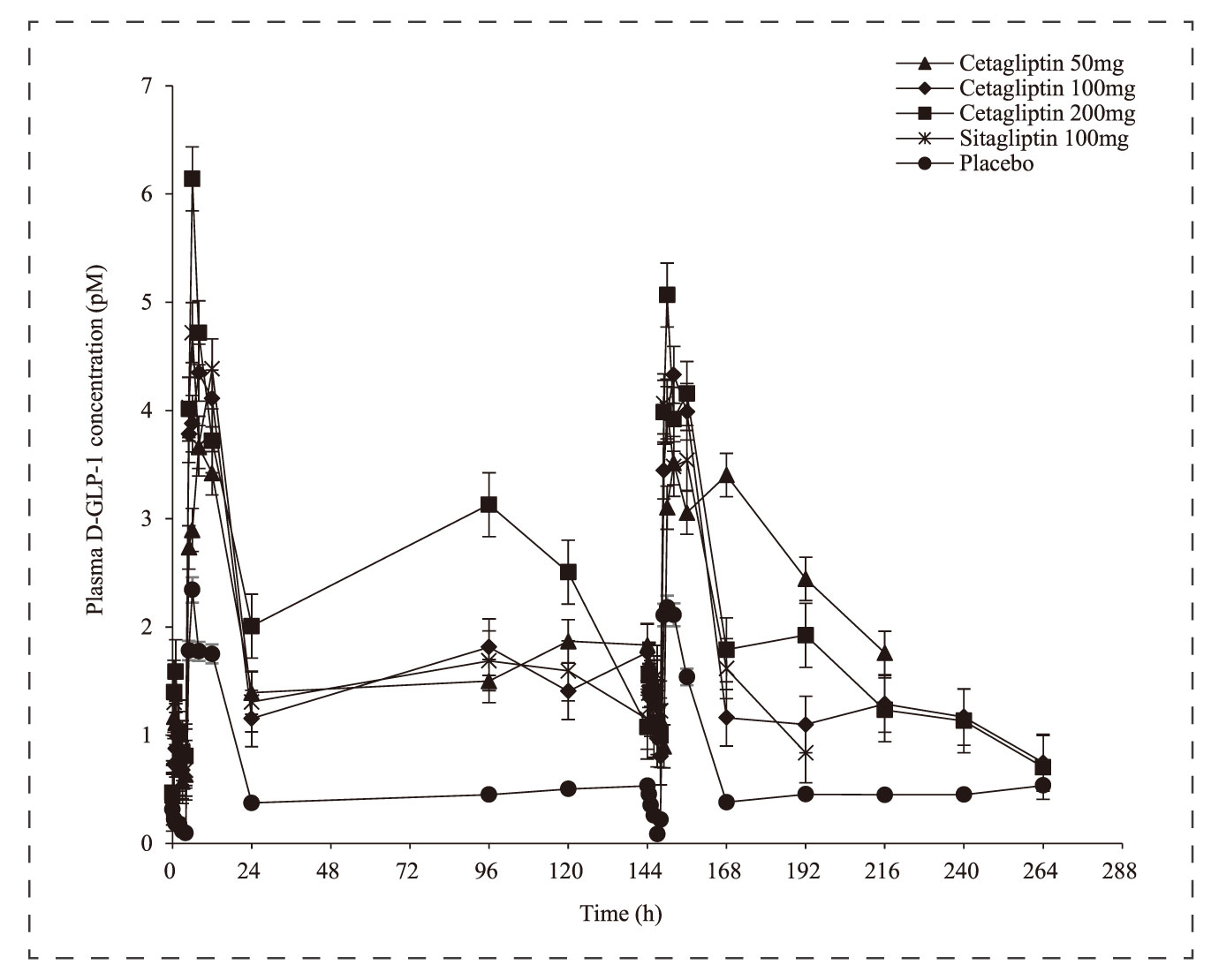 活性D-GLP-1检测[3]
活性D-GLP-1检测[3]
美迪西在GLP-1相关药物的体内分析中提供了多种高质量的测试方法,通过分析动物体内采集的血浆/血清样本,为客户提供可靠优质的PK数据。
 Compound A的药代动力学参数
实验结果显示血浆药物暴露量(Cmax 和AUC(0-t))的增加与给药剂量的增加比例基本一致。单次皮下给予0.04 mg/kg 的对照品注射液和0.04 mg/kg 的Compound A注射液后,相对生物利用度为83.17%。
Compound A的药代动力学参数
实验结果显示血浆药物暴露量(Cmax 和AUC(0-t))的增加与给药剂量的增加比例基本一致。单次皮下给予0.04 mg/kg 的对照品注射液和0.04 mg/kg 的Compound A注射液后,相对生物利用度为83.17%。
2022年9月30日,质肽生物研发的司美格鲁肽注射液获得CDE正式受理。质肽生物司美格鲁肽注射液,是一款完全对标Ozempic的新型长效胰高糖素样肽-1(GLP-1)生物类似物,用于在饮食控制和运动基础上,接受二甲双胍和/或磺脲类药物血糖不达标的成人2型糖尿病患者的血糖控制,及降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死或非致死性卒中)风险。每周注射1次,它能高效降糖、减重,并降低心脑血管发病率,是行业内公认的最优GLP-1品种。
作为质肽生物的合作伙伴,美迪西为质肽生物司美格鲁肽注射液提供了(包括药效、药代、安评在内的)等全套临床前研究服务。根据质肽生物的需求,美迪西凭借在代谢性疾病领域积累的丰富经验和有效的动物模型,为其制订了一系列严谨的试验方案,证实了其药效强度和持续作用与Ozempic完全吻合,并协调排期无缝对接一站式研发服务,全力确保了该项目高质高效的完成。
2022年8月29日,质肽生物的GLP-1超长效制剂注射液获得澳洲人类研究伦理委员会签发的Ⅰ期临床试验的许可。10月5日,质肽生物的该新药在澳洲完成 I 期临床首例受试者给药,该产品具有自主知识产权,主要治疗糖尿病和肥胖症等相关代谢性疾病。严格、系统的临床前研究证实了此超长效制剂与目前临床治疗应用长效GLP-1有相同疗效,但其更长的半衰期,有希望成为全球第一个每月仅给药一次的GLP-1R激动剂,这对糖尿病等慢性病患者具有里程碑意义,它将极大地改善病人治疗负担,显著提高患者的依从性,从而达到更好的治疗效果。
目前,此超长效制剂也已获CDE批准,开展糖尿病和减重治疗两项临床,阿尔兹海默症等适应症也在申报中,“预计会在2023年底完成Ⅰ期临床,2024年底完成Ⅱ期临床,有望在未来4-5年内获批上市”。此超长效制剂市场前景可观、潜力巨大,不仅证实了质肽生物作为“国家高新技术企业”硬核的创新能力、领先的研发水平,也充分彰显了质肽生物在代谢疾病领域蛋白类创新药物研发领域的领导地位!
作为质肽生物的合作伙伴,美迪西凭借新药临床前研究多年丰富的经验,与质肽生物保持紧密合作,以专业严谨的科研态度,对此超长效制剂项目进行详细分析,为其制定了科学合理的药效实验方案,从而获得了该产品应有的动物实验数据,为该产品提供了符合中、美、澳三国申报的药效服务,加速了海外临床申报进程。
2023年4月20日,据CDE官网,德睿智药科技MDR-001片获批临床,拟开展治疗2型糖尿病和肥胖或超重患者的体重管理的研究。MDR-001是德睿智药通过其AI驱动药物发现平台Molecule Pro开发的一款非竞争性口服GLP-1R小分子激动剂,已于2022年12月获FDA批准开展临床。临床前研究显示,MDR-001具有优异的药效和选择性,良好的ADME和口服生物利用度以及更优的药代动力学特征,具备best-in-class潜力。
MDR-001在临床前研究中表现出较为较好的药效和选择性,同时表现出良好的ADME(吸收、分布、代谢和排泄)、口服生物利用度及药代动力学特征。此外,临床前研究显示该药与多肽有近似的药效及更高的安全窗,同时无免疫原性、口服便利,有望给糖尿病和肥胖症患者带来更优的治疗选择。在早期的糖尿病合并肥胖猴的药效模型中,长期给药结果显示,MDR-001除了能有效降糖和降体重,还能使糖化血红蛋白(HbA1C)恢复到健康猴水平,而且停药后恢复期没有出现反弹,提示该药有助于修复受损胰岛细胞、恢复胰岛功能,显示出可以治愈早期糖尿病的潜力。
作为德睿智药的合作伙伴,美迪西为MDR-001提供了原料药工艺开发和制剂研发服务。在确保研发质量的基础上,美迪西通过严谨的试验方案设计、专业化的研发技术、标准化的项目管理、规范化的试验操作、高效的多方沟通,加速了研发进程,对这一重量级GLP-1R激动剂获批临床做出了自己的贡献。
GLP-1R激动剂作为新型降糖药物,不仅在降糖方面效果较好,同时还具有减轻体重、降压、降脂、心血管保护、肾脏保护、改善糖尿病视网膜病变预后等临床作用。期待未来有更多的基础研究和临床试验去发现GLP-1R激动剂更多的作用,为临床应用提供更为有效的证据。
作为国内CRO行业中少数具有综合服务能力的生物医药临床前研究企业,美迪西近20年来一直在追赶创新,洞察和最新技术发展,搭建全球创新药发展方向的技术服务平台,也助力新药加速注册申报。美迪西临床注册事务服务平台拥有专业的IND、ANDA研究团队,深入了解中国、美国、澳洲和欧盟等国家和地区的注册法规政策以及其对化学药物的技术要求,能为国内客户提供NMPA的IND申报、US FDA的IND/ANDA申报服务,能为国外客户提供NMPA的IND/ANDA申报服务,定制切实可行的注册策略,规避潜在的注册风险,确保及时准确的递交申报资料,还会跟踪审评进度,以便助力客户快速地完成注册审评流程。
[1] Baptist Gallwitz. The evolving place of incretin-based therapies in type 2 diabetes. Pediatr Nephrol. 2010 Jul;25(7):1207-17. doi: 10.1007/s00467-009-1435-z.
[2] Wenwei Wan, et al. GLP-1R Signaling and Functional Molecules in Incretin Therapy. Molecules.2023 Jan 11;28(2):751. doi: 10.3390/molecules28020751.[3] Jinmiao Lu, et al. A double-blind, randomized, placebo and positive-controlled study in healthy volunteers to evaluate pharmacokinetic and pharmacodynamic properties of multiple oral doses of Cetagliptin. Br J Clin Pharmacol. 2022 Jun;88(6):2946-2958. doi: 10.1111/bcp.15209.[4] André J Scheen. GLP-1 receptor agonists or DPP-4 inhibitors: how to guide the clinician? Ann Endocrinol (Paris).2013 Dec;74(5-6):515-22. doi: 10.1016/j.ando.2012.06.002.[5] Xin Zhao, et al. GLP-1 Receptor Agonists: Beyond Their Pancreatic Effects. Front Endocrinol (Lausanne).2021 Aug 23;12:721135. doi: 10.3389/fendo.2021.721135.
[6] Serap Koral Taşçı, et al. GLP-1 Localisation and Proglucagon Gene Expression in Healthy and Diabetic Mouse Ileum. J Vet Res. 2018 Oct 24;62(2):237-242. doi: 10.2478/jvetres-2018-0033.
 Compound A的药代动力学参数
Compound A的药代动力学参数